Патент на российскую вакцину рассматривается уже в 150 странах, заявил сегодня директор центра им. Гамалеи Александр Гинцбург, но в первую очередь средство должно покрыть внутренние нужды. В то же время ВОЗ не спешит признавать разработку, т. к. вакцина не прошла этап массовых клинических испытаний. О том, на сколько хватит иммунитета от прививки и как сами разработчики объясняют невероятную скорость получения результата, — в материале «БИЗНЕС Online».
 Директор центра им. Гамалеи Александр Гинцбург (на фото с министром здравоохранения РФ Михаилом Мурашко (справа) ожидает, что антиковидная прививка сможет защищать до двух лет
Директор центра им. Гамалеи Александр Гинцбург (на фото с министром здравоохранения РФ Михаилом Мурашко (справа) ожидает, что антиковидная прививка сможет защищать до двух лет
Новая вакцина начнет использоваться уже через ДВЕ недели. какие противопоказания?
Первые партии анонсированной накануне президентом России Владимиром Путиным вакцины против коронавируса будут выпущены уже в течение двух недель. Об этом сегодня заявил министр здравоохранения РФ Михаил Мурашко — по его словам, прививка станет добровольной (в том числе для медиков, которых будут вакцинировать в приоритетном порядке), а полное обеспечение России вакциной планируется в течение года. Интересно, что, как сообщил глава минздрава, для отслеживания нежелательных реакций у тех, кто получил вакцину от коронавируса, будет разработано мобильное приложение.
Напомним, первая в мире вакцина от COVID-19 получила название «Спутник V». Сообщается, что, по утверждению российских властей, она прошла все необходимые проверки, формирует устойчивый иммунитет. Производиться разработанный в институте им. Гамалеи препарат будет на фармацевтическом заводе «Биннофарм» в Зеленограде (входит в АФК «Система»), разработку и производство его финансирует российский фонд прямых инвестиций.
«Спутник V» (он же «Гам-Ковид-Вак») — это векторная вакцина, созданная с помощью генетической инженерии. Для такой вакцины выбирается безопасный для человека вирус, и в его геном встраивается ген того вируса, против которого делается вакцина. Продукт этого гена, белок, должен вызывать иммунитет против вируса – возбудителя болезни.
Как рассказал нашему изданию главный научный сотрудник Института биологии гена РАН Анатолий Альтштейн, она состоит из двух серотипов аденовируса, в геном которых встроен ген коронавируса SARS-CoV-2, кодирующий белок, отвечающий за выработку защитного иммунитета. «Такой аденовирус выращивается в культуре специальных клеток человека, в которых он прекрасно размножается и дает очень большое количество вирусных частиц (вирионов), содержащих коронавирусную генетическую вставку. Из этого вируса и готовится вакцина. Когда ее вводят в организм человека, вирус не способен размножаться. Подобным достигается высокая безопасность вакцины, такая же, как у инактивированных вакцин. Однако вирус сохраняет способность заразить клетки в организме вакцинированного и ввести в них свой генетический материал, содержащий и встроенный коронавирусный ген, который вызывает образование иммунизирующего коронавирусного белка. Организм реагирует на этот белок образованием иммунитета против коронавируса. Если вакцинированный человек встретится с коронавирусом, его иммунная система (антитела и иммунные клетки) подавит развитие инфекции», — объяснял эксперт.
Почему будут использованы два аденовируса, содержащие коронавирусную генетическую вставку? По словам Альтштейна, при введении первого аденовируса у человека образуются антитела не только против коронавирусного белка, но и против аденовируса. Для полного иммунного ответа нужно ввести вакцину повторно через две-три недели. Если сделать это тем же самым аденовирусом, то может быть проблема в виде образования антител не только против коронавируса, но и против вируса-вектора. «Если вы второй раз введете тот же вектор, антитела могут связать его и нарушить вакцинирующее действие. Чтобы этого не было, меняется тип вектора. У двух аденовирусов нет перекрестной нейтрализации антителами. Потому вторая инъекция будет эффективной и вызовет подъем иммунитета», — рассказывает ученый.
Точки над i расставил директор Национального исследовательского центра эпидемиологии и микробиологии им. Гамалеи Александр Гинцбург в большом интервью «Интерфаксу». Эксперт ожидает, что по аналогии с вакциной от лихорадки Эбола антиковидная прививка сможет защищать до двух лет — во всяком случае, у тех ученых центра, кто привился еще в марте, антитела сохраняются.
Ключевые тезисы выглядят следующим образом.
Этапы разработки в России и мире. Гинцбург рассказал, что сейчас зарегистрирована жидкая форма вакцины, а на следующей неделе ожидается регистрация лиофилизированной, сухой ее формы, которую удобнее транспортировать, но она гораздо дороже. «Есть еще китайская вакцина, она, по-моему, зарегистрирована для ограниченного применения в китайской армии. Остальные вакцины в мире находятся на различных стадиях клинических испытаний», — объяснил он расклад сил. Впрочем, через несколько часов после выхода интервью появились сообщения, что американская биотехнологическая компания Moderna Inc. договорилась с властями США о предоставлении 100 млн доз своей экспериментальной вакцины более чем за $1,5 миллиарда.
По словам ученого, оксфордская вакцина разрабатывается по той же технологии, что и российская («у них только аденовирус взят от обезьяны, а у нас — от человека»), однако он считает, что она не будет давать столь продолжительного иммунитета, как отечественная, двухкомпонентная.
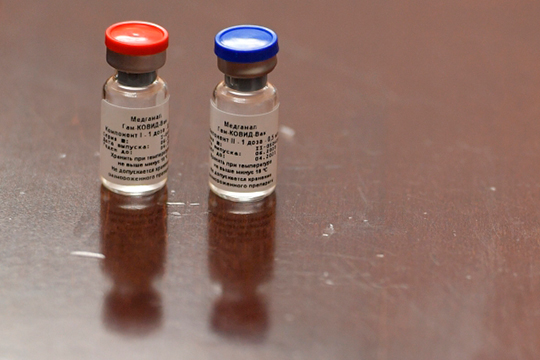 Оксфордская вакцина разрабатывается по той же технологии, что и российская («у них только аденовирус взят от обезьяны, а у нас — от человека»), однако Гинцбург считает, что она не будет давать столь продолжительного иммунитета
Оксфордская вакцина разрабатывается по той же технологии, что и российская («у них только аденовирус взят от обезьяны, а у нас — от человека»), однако Гинцбург считает, что она не будет давать столь продолжительного иммунитета
Побочные эффекты и противопоказания. Директор центра им. Гамалеи заверил, что вакцину проверяли на эмбриотоксичность (вред для плода во время беременности), опыты дали положительный результат. Тестирование на нескольких поколений животных не выявили противопоказаний. «Когда уже наступила беременность, думаю, особой необходимости нет в применении вакцины», — заявил он.
«Из противопоказаний — серьезные хронические аутоиммунные заболевания: артит, артроз, острые стадии, поллинозы, аллергия на продукты питания. Чтобы не обострить их, надо серьезно консультироваться с иммунологом — это как и с другими прививками, здесь никаких исключений нет», — объяснил Гинцбург. По его словам, после регистрации будет исследоваться возможность вакцинирования людей старше 60 лет, даже 90-летних. Исследование вакцины на детях сложнее и должно проходить в разбивке по группам: сначала 18–14 лет, дальше — 14–12, 12–8, причем каждая стадия занимает три-четыре месяца.
Скорость и качество. Ученый считает, что о безответственной поспешности говорить нельзя, потому что технологию разработки вакцины в центре начали создавать еще 25 лет назад и на ее основе до антиковидной было сделано еще две или три вакцины. «С 2014 года мы в течение 15 месяцев создали вакцину от Эболы и еще два ее варианта. Когда возникла пандемия коронавируса, мы уже фактически сделали вакцину от MERS. То есть в этот момент для создания вакцины от коронавируса нужно было только вставить другую последовательность в вектор („транспорт“ для доставки генетического материала в клетки), она на 80 процентов гомологична уже испытанной вакцине», — объяснил он. По его словам, у других фармкомпаний не было достаточного количества компонентов, кто-то использовал аденовирус у обезьян, который ранее не применялся в зарегистрированных вакцинах, а кто-то решил создать принципиально новую систему доставки РНК внутрь клеток.
«Роспатент оперативно и быстро провел все необходимые процедуры, чтобы дать положительное решение», — отметил Гинцбург. Так что месяц назад была подана международная заявка, которая рассматривается уже в 150 странах, где — в случае положительного решения — появится возможность наладить производство. «Если патент купят, будем получать роялти», — заключил эксперт.
«ФОНТАНКА»: В ДОКУМЕНТАХ 144 «ПОБОЧКИ» НА 38 ДОБРОВОЛЬЦЕВ
Однако в документах центра им. Гамалеи, с которыми ознакомилась «Фонтанка», все не так радужно. Издание пишет: «Вакцина прошла процедуру регистрации препаратов, применяемых только в условиях возникновения ЧС». При этом места вакцинации должны быть оснащены средствами противошоковой терапии.
Иммунологические свойства и безопасность изучали только на взрослых здоровых добровольцах в количестве 38 человек на протяжении 42 дней, поэтому до конца защитные свойства не исследованы. «Защитный титр в настоящее время неизвестен, как и продолжительность защиты. Клинические исследования по изучению эпидемиологической эффективности не проводились», — приводит издание содержание отчета. Отмечается, что на 42-е сутки с момента вакцинации в сыворотке крови всех добровольцев выявлены вируснейтрализующие антитела к вирусу со средним титром 49,3.
Притом надо иметь в виду, что титр — это предельное разведение сыворотки крови, при котором могут быть обнаружены антитела, а показатель в 49,3 меньше среднего уровня антител, пишет издание, уточняя, что со временем он может уменьшиться еще сильнее.
Но даже это не самое интересное. Обращают на себя внимание показатели безопасности, которые, мягко говоря, настораживают. «У 38 подопытных было зафиксировано 144 нежелательных явления. Большинство прошло без последствий. Однако на 42-й день исследования не завершилось 31 нежелательное явление (были зарегистрированы лабораторные отклонения иммунологических показателей). Исход 27 нежелательных явлений разработчику до сих пор не известен, следует из документов», — пишет издание, сообщая, что у добровольцев после вакцинации были зафиксированы отечность, боль, гипертермия и зуд в месте введения препарата, а из общих проявлений — астения, недомогание, пирексия, повышение температуры, снижение аппетита, головная боль, диарея, боль в ротоглотке, заложенность носа, першение в горле, ринорея.
По данным «Фонтанки», документы центра им. Гамалеи, сформированные на основе открытого клинического исследования безопасности, не подтверждают тезис об отсутствии побочных эффектов, в чем уверяли многие эксперты. «Специалисты признали, что нежелательные явления (НЯ) по частоте встречаемости могут быть расценены как встречающиеся часто и очень часто», — говорится в статье.
Ну и напоследок отмечается чувствительность самого препарата: выяснилось, что его следует хранить в замороженном виде, при температуре не выше минус 18 градусов, перед применением выдержать при комнатной температуре, «но не дольше 30 минут». Резко встряхивать ампулу не допускается, как и замораживать повторно. Неудивительно, что центр так активно работает над регистрацией сухого варианта «Спутника».
«Медуза» при этом обращает внимание на то, что разработчики так и не опубликовали подробности испытания вакцины ни в одном научном журнале, а до завершения полноценных исследований третьей фазы вопрос о том, эффективна вакцина или нет, остается открытым. Дело в том, что испытания лекарств регулярно проваливаются на этом этапе.
Так что, делает вывод издание, те, кто будет прививаться данной вакциной, делают это фактически на свой страх и риск: «Они не обязаны подписывать соответствующие бумаги, вести дневник добровольца, их не защищает Хельсинкская декларация, а производитель не обязан следить за состоянием людей и включать данные по ним в исследование».
 Месяц назад была подана международная заявка, которая рассматривается уже в 150 странах, где — в случае положительного решения — появится возможность наладить производство. «Если патент купят, будем получать роялти», — отметил Гинцбург
Месяц назад была подана международная заявка, которая рассматривается уже в 150 странах, где — в случае положительного решения — появится возможность наладить производство. «Если патент купят, будем получать роялти», — отметил Гинцбург
Реакция мира: сомнения в безопасности или боязнь конкуренции?
Международное сообщество отреагировало на регистрацию вакцины довольно эмоционально. Основная претензия заключалась в том, что Россия сократила этапы тестирования вакцины, что, по мнению ряда стран, может сказаться на безопасности. Отмечается, что такие компании, как Moderna, Pfizer/BioNTech, Оксфордский университет / AstraZeneca, Sinopharm / Уханьский институт биопрепаратов, китайский Sinovac, CanSinoBio, приступили к третьему этапу тестирования, который в России начнется только 12 августа.
Так, сегодня на обложке французского журнала Libération разместили портрет Путина в костюме Джеймса Бонда со шприцем в руках вместо пистолета. Заголовок: «Вакцина против COVID. Завтра не умрет никогда». Внутри большая статья о новой вакцине на четырех полосах и объяснение, почему ее назвали «Спутник» («В честь искусственного спутника, который удивил весь мир, обогнав в октябре 1957 года американцев в комической гонке»). Там же размещен материал швейцарского ученого – генетика Франсуа Баллу, который называет быстрое появление вакцины опасным следствием «политического решения, применяемого в рамках бешеной гонки вооружений (по разработке) вакцины от коронавируса». Он пишет, что Россия отказалась от международных консенсусов и тем самым «пренебрегла международными стандартами».
Директор Национального института аллергических и инфекционных заболеваний США Энтони Фаучи во время экспертной дискуссии, организованной телеканалом National Geographic, выразил серьезные сомнения в том, что вакцина будет безопасной. «Я надеюсь, что россияне точно подтвердили безопасность и эффективность вакцины. У меня есть серьезные сомнения в том, что они сделали это», — сказал он, отметив, что США работает над 6 или больше вакцинами. «Если бы мы хотели рискнуть и навредить множеству людей, дав им то, что не работает, то могли бы при желании начать хоть на следующей неделе. Однако это действует не так», — пояснил эксперт.
С ним солидарен и министр здравоохранения Германии Йенс Шпан, который тоже довольно скептически прокомментировал новости о российском препарате. Он считает, что лекарство пока не прошло третью стадию клинических исследований на большой выборке добровольцев, поэтому «вакцинировать миллионы или даже миллиарды человек» слишком рано и, вероятно, опасно, передает его слова РИА «Новости».
Президент Сербии Александар Вучич заявил, что готов первым получить российскую вакцину от коронавируса, «когда сербские специалисты скажут, что она хорошая». «Я счастлив, если русские произвели вакцину, которая ожидалась до ноября. Только наши специалисты должны подтвердить нам, что она безопасна и надежна. Важно, чтобы вакцина появилась как можно скорее, потому что это спасение для нашей экономики», — заявил он (цитата по ТАСС).
В ВОЗ же заявили, что ждут дополнительных данных по этой разработке и гарантий безопасности нового препарата. «Преквалификация ВОЗ любой вакцины включает в себя скрупулезное рассмотрение и оценку всех необходимых данных по безопасности и эффективности, полученных в ходе клинических испытаний», — передает «Интерфакс» комментарии технических экспертов ВОЗ. При этом там отметили: «Любая конечная вакцина станет общественным благом мирового масштаба, и ВОЗ призывает предоставить быстрый, справедливый и равный доступ к вакцинам от коронавируса по всему миру в соответствии с принципом „никто не должен остаться в стороне“». «Солидарность — ключ в этом процессе», — заявили в ВОЗ.
«Коллеги зарубежные, которые, видимо, чувствуя определенную конкуренцию, конкурентные преимущества российского препарата, пытаются высказывать какие-то мнения, которые, на наш взгляд, абсолютно безосновательны. <…> Но российская вакцина (еще раз говорю) — это решение, которое уже имело определенные клинические знания и данные», — отреагировал Мурашко на критику вакцины во время сегодняшнего брифинга.
«вакцина, о которой мы говорим, генно-инженерная. Еще лет 35–40 назад это было фантастикой»
Мы попросили экспертов оценить обоснованность претензий
Михаил Щелканов — НИИ вирусологии им. Ивановского, профессор, вирусолог:
— Тут даже думать нечего. Вакцина зарегистрирована в соответствии с санитарными правилами и законодательством РФ, это не подлежит сомнению. Что касается зарубежной критики, то в других странах могут быть другие правила, ведь подобное регулируется национальным законодательством. Если там другие правила — ну извините, в чужой монастырь со своим уставом не ходят. Я не вижу смысла обсуждать нашу регистрацию с точки зрения законодательства других стран.
Мой тезис ясен и понятен: регистрацией первой в мире вакцины Российская Федерация доказала, что она способна оперативно, в кратчайшие сроки производить эффективные и безопасные вакцины. РФ всегда со времен СССР была лидером в области вакцинологии. В 90-е годы мы рухнули, но с начала 2000-х собрались и в критических точках развития не только достигли мирового уровня, но и, в общем, являемся лидерами, и регистрация вакцины от COVID-19 еще раз это подтверждает. Считать, что наши стандарты чем-то хуже, по меньшей мере наивно и непрофессионально.
То, что с апреля в России стал необязателен третий этап исследований для регистрации вакцины, сделано не просто росчерком пера. Проведен глубокий анализ существующего положения дел, и, если эксперты сочли (я, кстати, сам выступал за это) подобное возможным, значит, так, потому что наука тоже не стоит на месте, появляются новые технологии. В частности, та вакцина, о которой мы говорим, генно-инженерная. Еще лет 35–40 назад это было фантастикой, а сейчас норма жизни. Потому естественно, что и наше законодательство, и наши платформы должны соответствовать передовым идеям в области вирусологии. Я здесь не вижу никакого повода для сомнений.
Екатерина Зеленцова — вирусолог клиники «Ихилов», Израиль:
— Должно обязательно пройти определенное время, в течение которого вакцина обязана тестироваться. И страны, которые начали разрабатывать вакцину почти сразу, сейчас находятся только на третьем этапе. Как такое возможно, что Россия прыгнула и сократила какой-то этап? ВОЗ в принципе запрещает уменьшать этапы, и даже в условиях сильной пандемии нельзя сокращать исследования на целый этап. Ради безопасности прививки должно пройти тестирование определенное количество людей. Я считаю, что сомнения мирового сообщества в безопасности российской вакцины обоснованны.

Внимание!
Комментирование временно доступно только для зарегистрированных пользователей.
Подробнее
Комментарии 138
Редакция оставляет за собой право отказать в публикации вашего комментария.
Правила модерирования.